Produkty
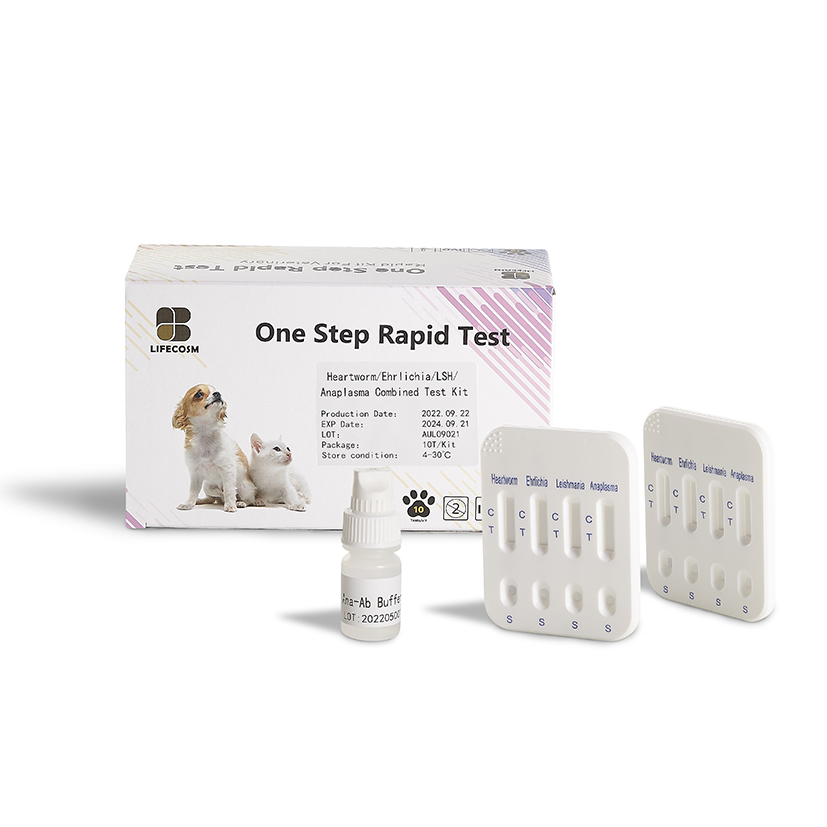
Zestaw testowy Lifecosm CHW Ag/Anaplasma Ab/E.canis Ab/LSH Ab
Zestaw testowy CHW Ag/Anaplasma Ab/E.canis Ab/LSH Ab na obecność nicieni sercowych u psów, Ag/Anaplasma Ab /Ehrlichia canis Ab/Leishmania Ab
| Numer katalogowy | RC-CF31 |
| Streszczenie | Wykrywanie antygenów Dirofilaria immitis u psów, przeciwciał Anaplasma, przeciwciał E. canis i przeciwciał LSH w ciągu 10 minut |
| Zasada | Jednoetapowy test immunochromatograficzny |
| Cele wykrywania | CHW Ag: antygeny Dirofilaria immitis Anapalsma Ab: przeciwciała AnaplasmaE. canis Ab: Przeciwciała E. canis LSH Ab: L. chagasi, L. infantum i L. donovani przeciwciała |
| Próbka | Pełna krew, osocze lub surowica dla psów |
| Czas czytania | 10 minut |
| Ilość | 1 pudełko (zestaw) = 10 urządzeń (Opakowanie indywidualne) |
| Zawartość | Zestaw testowy, butelka z buforem i jednorazowy kroplomierz |
| Składowanie | Temperatura pokojowa (2 ~ 30℃) |
| Wygaśnięcie | 24 miesiące od daty produkcji |
| Ostrożność | Zużyć w ciągu 10 minut po otwarciu.Użyj odpowiedniej ilości próbki (0,01 ml kroplomierza) Jeśli były przechowywane w chłodnym miejscu, należy je zużyć po 15–30 minutach w temperaturze pokojowej. Po 10 minutach wyniki testu należy uznać za nieważne |
Informacja
Dorosłe nicienie sercowe osiągają długość kilku cali i zamieszkują tętnice płucne, gdzie mogą uzyskać wystarczającą ilość składników odżywczych. Nicienie sercowe wewnątrz tętnic wywołują stan zapalny i tworzą krwiaki. Serce powinno więc pompować krew częściej niż wcześniej, ponieważ liczba nicieni sercowych wzrasta, blokując tętnice.
Gdy stan zakażenia ulega pogorszeniu (u psa o wadze 18 kg żyje ponad 25 nicieni serca), nicienie te przedostają się do prawego przedsionka, blokując przepływ krwi.
Gdy liczba nicieni serca przekroczy 50, mogą one zająć
przedsionki i komory.
Po zakażeniu ponad 100 nicieniami serca w prawej części serca pies traci funkcję serca i ostatecznie umiera. Ta śmiertelna
Zjawisko to nazywane jest „syndromem żyły głównej”.
W przeciwieństwie do innych pasożytów, nicienie sercowe składają małe owady zwane mikrofilariami. Mikrofilarie u komarów przenoszą się do psa, gdy komar ssie jego krew. Nicienie sercowe, które mogą przetrwać w żywicielu przez 2 lata, giną, jeśli nie przeniosą się do innego żywiciela w tym okresie. Pasożyty bytujące w ciężarnej suce mogą zainfekować jej zarodek.
Wczesne badanie nicieni serca jest bardzo ważne w celu ich wyeliminowania. Nicienie serca przechodzą przez kilka etapów, takich jak L1, L2, L3, w tym etap transmisji przez komara, aby stać się dorosłymi nicieniami serca.
Robaki serca u komarów
Mikrofilarie u komarów rozwijają się w pasożyty L2 i L3, które są w stanie zainfekować psy w ciągu kilku tygodni. Wzrost zależy od pogody. Sprzyjająca temperatura dla pasożyta wynosi ponad 13,9℃.
Kiedy zainfekowany komar ugryzie psa, mikrofilarie L3 wnikają w jego skórę. W skórze mikrofilarie rozwijają się w L4 przez 1~2 tygodnie. Po 3 miesiącach przebywania w skórze L4 rozwija się w L5, który przemieszcza się do krwi.
L5 to postać dorosła nicienia sercowego, który przedostaje się do serca i tętnic płucnych, gdzie po 5–7 miesiącach nicienie sercowe składają owady.


Diagnoza
Przy diagnozowaniu psa należy wziąć pod uwagę historię choroby i dane kliniczne chorego psa oraz różne metody diagnostyczne. Na przykład wymagane jest prześwietlenie rentgenowskie, badanie USG, badanie krwi, wykrycie mikrofilarii, a w najgorszym przypadku sekcja zwłok.
Badanie surowicy;
Wykrywanie przeciwciał lub antygenów we krwi
Badanie antygenowe;
Koncentruje się na wykrywaniu specyficznych antygenów żeńskich dorosłych nicieni sercowych. Badanie przeprowadzane jest w szpitalu, a jego wskaźnik powodzenia jest wysoki. Zestawy testowe dostępne na rynku są zaprojektowane do wykrywania dorosłych nicieni sercowych w wieku 7–8 miesięcy, więc nicienie sercowe młodsze niż 5 miesięcy są trudne do wykrycia.
Leczenie
W większości przypadków infekcja nicieniami serca jest skutecznie leczona. Aby wyeliminować wszystkie nicienie serca, najlepszym sposobem jest stosowanie leków. Wczesne wykrycie nicieni serca zwiększa wskaźnik powodzenia leczenia. Jednak w późnym stadium infekcji mogą wystąpić powikłania, które utrudniają leczenie.
Informacja
Bakteria Anaplasma phagocytophilum (dawniej Ehrilichia phagocytophila) może powodować zakażenia u kilku gatunków zwierząt, w tym u ludzi. Choroba u przeżuwaczy domowych nazywana jest również gorączką przenoszoną przez kleszcze (TBF) i jest znana od co najmniej 200 lat. Bakterie z rodziny Anaplasmataceae to gram-ujemne, nieruchome, ziarniakowate do elipsoidalnych organizmy, o średnicy od 0,2 do 2,0 um. Są obligatoryjnymi tlenowcami, pozbawionymi szlaku glikolizy i wszystkie są obligatoryjnymi pasożytami wewnątrzkomórkowymi. Wszystkie gatunki z rodzaju Anaplasma zamieszkują wyścielone błoną wakuole w niedojrzałych lub dojrzałych komórkach hematopoetycznych gospodarza ssaka. Fagocytophilum infekuje neutrofile, a termin granulocytotropowy odnosi się do zakażonych neutrofili. Rzadko organizmy, zostały znalezione w eozynofilach.
Anaplasma phagocytophilum
Objawy
Typowe objawy kliniczneanaplazmoza u psów obejmuje wysoką gorączkę, letarg, depresję i zapalenie wielostawowe. Mogą być również widoczne objawy neurologiczne (ataksja, drgawki i ból szyi). Zakażenie Anaplasma phagocytophilum rzadko jest śmiertelne, chyba że jest powikłane innymi zakażeniami. Bezpośrednie straty, stany wyniszczające i straty produkcyjne obserwowano u jagniąt. Odnotowano poronienia i zaburzenia spermatogenezy u owiec i bydła. Na ciężkość zakażenia wpływa kilka czynników, takich jak zaangażowane warianty Anaplasma phagocytophilum, inne patogeny, wiek, stan odporności i kondycja żywiciela oraz czynniki takie jak klimat i zarządzanie. Należy wspomnieć, że objawy kliniczne u ludzi wahają się od łagodnej, samoograniczonej choroby grypopodobnej do zakażenia zagrażającego życiu. Jednak większość zakażeń u ludzi prawdopodobnie powoduje minimalne lub żadne objawy kliniczne.
Przenoszenie
Anaplasma phagocytophilum jest przenoszona przez kleszcze ixodidowe. W Stanach Zjednoczonych głównymi wektorami są Ixodes scapularis i Ixodes pacificus, podczas gdy Ixode ricinus okazał się być głównym wektorem egzofilnym w Europie. Anaplasma phagocytophilum jest przenoszona transstadialnie przez te kleszcze-wektory i nie ma dowodów na transmisję transowarialną. Większość dotychczasowych badań, które badały znaczenie ssaczych żywicieli A. phagocytophilum i jego kleszczy-wektorów, koncentrowała się na gryzoniach, ale ten organizm ma szeroki zakres żywicieli ssaczych, zakażając udomowione koty, psy, owce, krowy i konie.

Diagnoza
Pośredni test immunofluorescencyjny jest głównym testem stosowanym do wykrywania infekcji. Próbki surowicy w fazie ostrej i rekonwalescencji można ocenić pod kątem czterokrotnej zmiany miana przeciwciał przeciwko Anaplasma phagocytophilum. Wewnątrzkomórkowe inkluzje (morulea) są widoczne w granulocytach na rozmazach krwi barwionych metodą Wrighta lub Gimsy. Metody reakcji łańcuchowej polimerazy (PCR) są stosowane do wykrywania DNA Anaplasma phagocytophilum.
Zapobieganie
Nie ma szczepionki zapobiegającej zakażeniu Anaplasma phagocytophilum. Zapobieganie polega na unikaniu narażenia na kleszcze (Ixodes scapularis, Ixodes pacificus i Ixode ricinus) od wiosny do jesieni, profilaktycznym stosowaniu środków przeciwkarycydowych i profilaktycznym stosowaniu doksycykliny lub tetracykliny podczas odwiedzania regionów endemicznych dla kleszczy Ixodes scapularis, Ixodes pacificus i Ixode ricinus.
Informacja
Ehrlichia canis to mały i prętowaty pasożyt przenoszony przez brązowego kleszcza psiego, Rhipicephalus sanguineus. E. canis jest przyczyną klasycznej erlichiozy u psów. Psy mogą być zarażone kilkoma gatunkami Ehrlichia, ale najczęstszą przyczyną erlichiozy u psów jest E. canis.
Wiadomo, że E. canis rozprzestrzenił się w całych Stanach Zjednoczonych, Europie, Ameryce Południowej, Azji i basenie Morza Śródziemnego.
Zakażone psy, które nie są leczone, mogą przez lata być bezobjawowymi nosicielami choroby i ostatecznie umrzeć na skutek masywnego krwotoku.

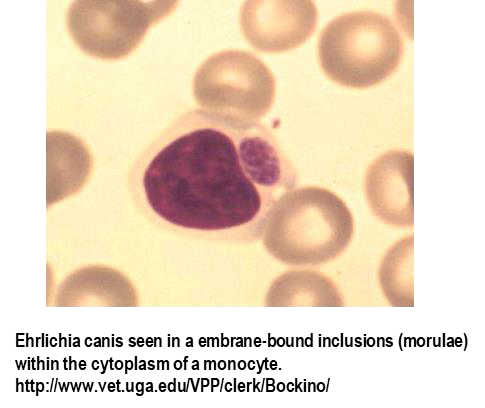
Objawy
Zakażenie Ehrlichia canis u psów dzieli się na 3 stadia;
FAZA OSTRA: Jest to zazwyczaj bardzo łagodna faza. Pies będzie apatyczny, nie będzie jadł i może mieć powiększone węzły chłonne. Może również wystąpić gorączka, ale rzadko ta faza zabija psa. Większość usuwa organizm samodzielnie, ale niektóre przechodzą do następnej fazy.
FAZA PODKLINICZNA: W tej fazie pies wygląda normalnie. Organizm odizolował się w śledzionie i zasadniczo się tam ukrywa.
FAZA PRZEWLEKŁA: W tej fazie pies znów zachoruje. Do 60% psów zarażonych E. canis będzie miało nieprawidłowe krwawienie z powodu zmniejszonej liczby płytek krwi. Głębokie zapalenie oczu zwane „zapaleniem błony naczyniowej oka” może wystąpić w wyniku długotrwałej stymulacji immunologicznej. Mogą być również widoczne efekty neurologiczne.
Diagnoza i leczenie
Ostateczna diagnoza Ehrlichia canis wymaga uwidocznienia moruli w monocytach w badaniu cytologicznym, wykrycia przeciwciał E. canis w surowicy za pomocą pośredniego testu immunofluorescencyjnego (IFA), amplifikacji reakcji łańcuchowej polimerazy (PCR) i/lub blottingu żelowego (immunoblotting Western).
Podstawą zapobiegania erlichiozy u psów jest zwalczanie kleszczy. Lekiem z wyboru w leczeniu wszystkich postaci erlichiozy jest doksycyklina stosowana przez co najmniej miesiąc. W ciągu 24–48 godzin od rozpoczęcia leczenia u psów z ostrą fazą choroby lub łagodną fazą przewlekłą powinna nastąpić drastyczna poprawa kliniczna. W tym czasie liczba płytek krwi zaczyna wzrastać i powinna powrócić do normy w ciągu 14 dni od rozpoczęcia leczenia.
Po zakażeniu możliwe jest ponowne zakażenie; odporność nie utrzymuje się po przebytym zakażeniu.
Zapobieganie
Najlepszą profilaktyką erlichiozy jest trzymanie psów z dala od kleszczy. Powinno to obejmować codzienne sprawdzanie skóry pod kątem kleszczy i leczenie psów środkami przeciwkleszczowymi. Ponieważ kleszcze przenoszą inne wyniszczające choroby, takie jak borelioza, anaplazmoza i gorączka plamista Gór Skalistych, ważne jest, aby psy były wolne od kleszczy.
Informacja
Leiszmanioza jest poważną i ciężką chorobą pasożytniczą ludzi, psów i kotów. Czynnikiem wywołującym leiszmaniozę jest pierwotniak pasożytniczy należący do kompleksu Leishmania donovani. Pasożyt ten jest szeroko rozpowszechniony w krajach strefy umiarkowanej i subtropikalnej Europy Południowej, Afryki, Azji, Ameryki Południowej i Ameryki Środkowej. Leishmania donovani infantum (L. infantum) jest odpowiedzialna za chorobę kotów i psów w Europie Południowej, Afryce i Azji. Leiszmanioza psów jest poważną postępującą chorobą układową. Nie u wszystkich psów rozwija się choroba kliniczna po zaszczepieniu pasożytami. Rozwój choroby klinicznej zależy od rodzaju odpowiedzi immunologicznej, jaką mają poszczególne zwierzęta.
przeciwko pasożytom.
Objawy
W psie
U psów mogą występować jednocześnie objawy trzewne i skórne; w przeciwieństwie do ludzi, nie obserwuje się oddzielnych zespołów skórnych i trzewnych. Objawy kliniczne są zmienne i mogą przypominać inne zakażenia. Mogą również występować zakażenia bezobjawowe. Typowe objawy trzewne mogą obejmować gorączkę (która może być okresowa), anemię, limfadenopatię, splenomegalię, letarg, zmniejszoną tolerancję wysiłku, utratę wagi i zmniejszony apetyt. Mniej powszechne objawy trzewne obejmują biegunkę, wymioty, smoliste stolce, kłębuszkowe zapalenie nerek, niewydolność wątroby, krwawienie z nosa, wielomocz-wielodypsję, kichanie, kulawiznę (z powodu zapalenia wielostawowego lub mięśni), wodobrzusze i przewlekłe zapalenie okrężnicy.
W kocim
Koty są rzadko zarażane. U większości zarażonych kotów zmiany ograniczają się do owrzodzeń skórnych z strupami, zwykle występujących na wargach, nosie, powiekach lub małżowinach usznych. Zmiany i objawy trzewne są rzadkie.
Cykl życia
Cykl życia kończy się u dwóch żywicieli. Żywiciela kręgowego i żywiciela bezkręgowego (mucha piaskowa). Samica muchy piaskowej żywi się żywicielem kręgowym ipołyka amastigoty. W owadzie rozwijają się wiciowce promastigoty. Promastigoty są wstrzykiwane do żywiciela kręgowego podczas karmienia muchówki. Promastigoty rozwijają się w amastigoty i rozmnażają się głównie w makrofagach. Rozmnażanie w makrofagach skóry, błon śluzowych i trzewi powoduje odpowiednio leiszmaniozę skórną, śluzówkową i trzewną
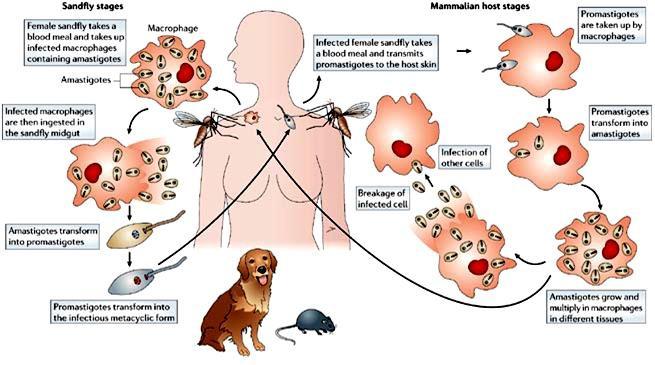
Diagnoza
U psów leiszmaniozę zazwyczaj diagnozuje się poprzez bezpośrednią obserwację pasożytów, stosując metodę Giemsy lub zastrzeżone szybkie barwienia, w rozmazach z węzłów chłonnych, śledziony lub aspiratów szpiku kostnego, biopsjach tkanek lub zeskrobinach skóry ze zmian. Organizmy można również znaleźć w zmianach ocznych, szczególnie w ziarniniakach. Amastigoty to pasożyty okrągłe lub owalne, z okrągłym jądrem zasadochłonnym i małym kinetoplastycznym prętem. Występują w makrofagach lub uwalniane z pękniętych komórek. Stosuje się również techniki immunohistochemiczne i łańcuchową reakcję polimerazy (PCR).
Zapobieganie
Najczęściej stosowanymi lekami są: antymonian megluminy w połączeniu z allopurynolem, aminozydyna, a ostatnio amfoterycyna B. Wszystkie te leki wymagają schematu wielokrotnych dawek, a to będzie zależeć od stanu pacjenta i współpracy właściciela. Zaleca się, aby leczenie podtrzymujące było kontynuowane allopurynolem, ponieważ nie można zagwarantować, że u psów nie nastąpi nawrót choroby, jeśli leczenie zostanie przerwane. U wszystkich pacjentów poddawanych leczeniu należy stale stosować obroże zawierające insektycydy, szampony lub spraye skutecznie chroniące psy przed ukąszeniami muchówek. Kontrola wektorów jest jednym z najważniejszych aspektów zwalczania chorób.
Muchówka jest wrażliwa na te same insektycydy, co przenoszący malarię.